I probiotici rappresentano un potenziale approccio terapeutico innovativo nel trattamento della depressione, agendo in modo mirato e simultaneo su specifici disturbi metabolici spesso associati a disbiosi del microbiota intestinale. Il trial clinico randomizzato PRO-DEMET ha valutato l’efficacia di una formulazione probiotica composta da ceppi selezionati, con l’obiettivo di indagare l’influenza sullo stato depressivo e su determinati parametri metabolici.
Lo studio si distingue per un protocollo solido, dal punto di vista metodologico, sulle cui basi sono stati sviluppati un’indagine pilota e un successivo studio principale (Gawlik-Kotelnicka et al., 2021; 2023; 2024), i cui risultati forniscono indicazioni rilevanti per ottimizzare gli interventi probiotici nel trattamento della depressione, in particolare in soggetti con profili metabolici specifici (1,2,3).
PRO-DEMET, descrizione dello studio
La ricerca ‘The Influence of Probiotic Supplementation on Depressive Symptoms, Inflammation and Oxidative Stress Parameters and Faecal Microbiota in Patients With Depression Depending on Metabolic Syndrome Comorbidity‘ (PRO-DEMET) è uno studio d’intervento (Randomized Controlled Trial, RCT) compiuto in Polonia nella città di Łódź (pronunciata ‘Wootch’) tra dicembre 2020 e maggio 2023. Lo studio è stato regolarmente inserito presso il database statunitense dei trial clinici. (4)
La preparazione probiotica utilizzata contiene i batteri lattici Lactobacillus helveticus Rosell®-52 e Bifidobacterium longum Rosell®-175. La scelta di questi ceppi si basa su evidenze preliminari emerse da precedenti studi di intervento e sperimentazioni su modelli animali, che ne hanno evidenziato la potenziale efficacia nel modulare l’asse microbiota–intestino–cervello sia in soggetti sani sia in pazienti affetti da depressione.
La sperimentazione ha avuto l’obiettivo di identificare una potenziale opzione terapeutica sicura e di facile utilizzo, da utilizzare come terapia aggiuntiva in una sotto-popolazione di pazienti depressi che rispondono solo parzialmente al trattamento farmacologico. L’ipotesi di base è che la comorbilità di depressione e sindrome metabolica aumenti la probabilità dell’effetto terapeutico dell’integrazione di probiotici in caso di sintomi depressivi e ansiosi attraverso l’aumento della diversità del microbiota fecale e quindi della sintesi di acidi grassi a catena corta (SCFA).
Protocollo di ricerca
Lo studio è di tipo prospettico, randomizzato, in doppio cieco e controllato a quattro bracci, a gruppi paralleli, che ha incluso 200 partecipanti per una durata di 20 settimane. I parametri valutati hanno incluso:
- variabili psicologiche e di qualità della vita (livelli di depressione, ansia, stress e qualità della vita);
- parametri antropometrici e cardiovascolari (pressione arteriosa, indice di massa corporea e circonferenza vita);
- indicatori ematologici e biochimici (conta leucocitaria, livelli sierici di proteina C-reattiva, colesterolo HDL, trigliceridi e glicemia a digiuno);
- profili del microbiota intestinale (composizione e livelli di specifici metaboliti fecali); e infine
- marcatori sistemici di infiammazione e stress ossidativo nel siero.
La selezione dei pazienti, effettuata nel rispetto dei criteri di eleggibilità prestabiliti, è avvenuta tramite randomizzazione 1:1, in cieco, sulla base della presenza o assenza di sindrome metabolica. Questo ha permesso la formazione di quattro gruppi distinti, così denominati:
- PRO-DMS. Probiotici + depressione + sindrome metabolica;
- PLC-DMS. Placebo + depressione + sindrome metabolica;
- PRO-D. Probiotici + depressione;
- PLC-D. Placebo + depressione.
L’intervento ha previsto il mantenimento delle normali abitudini alimentari e di attività fisica da parte dei partecipanti, al fine di ottenere una valutazione basale attendibile. I gruppi trattati con probiotici si distinguevano dal gruppo placebo esclusivamente per la presenza dei ceppi microbici attivi nelle capsule, identiche per eccipienti e aspetto esteriore. Gli esiti sono stati analizzati sulla base dei dati raccolti tramite questionari autosomministrati e dall’analisi di campioni biologici (sangue e feci) forniti dai partecipanti.
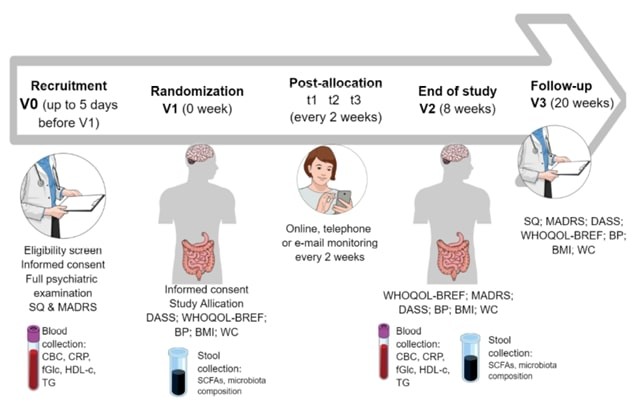
Fig. 1 – Overview dell’esecuzione dello studio PRO-DEMET (fonte: Gawlik-Kotelnicka et al., 2021). (5)
Risultati dello studio pilota
Lo studio pilota ha consentito di verificare la validità dell’ipotesi di partenza, in vista della sua estensione a un RCT completo. Tuttavia, sono emerse alcune limitazioni legate principalmente alla selezione dei partecipanti, ostacolata dalla pandemia e dalla distribuzione dei partecipanti affetti da sindrome metabolica nei gruppi di riferimento, non omogenea a causa della sua scarsa prevalenza nel campione complessivo (27%).
La composizione dei gruppi non ha mostrato differenze rilevanti in termini di sesso, età, diagnosi psichiatrica o trattamenti farmacologici. Anche le abitudini alimentari di base si sono rivelate abbastanza simili, ad eccezione del consumo di latticini e uova, che tuttavia non ha prodotto effetti significativamente differenti né sui punteggi psicometrici né sui marcatori metabolici e infiammatori all’inizio dell’intervento.
I risultati dello studio pilota sono stati utilizzati per ottimizzare il disegno dello studio principale, con l’obiettivo di aumentare la significatività statistica e ridurre le potenziali fonti di distorsione nell’effetto del trattamento, come il bias di selezione o il dropout selettivo (es. numero di partecipanti con sindrome metabolica).
Risultati dello studio principale
Lo studio principale ha coinvolto 116 pazienti, reclutati presso cliniche di assistenza primaria e ambulatori psichiatrici. I criteri di inclusione prevedevano una diagnosi di disturbo depressivo e un punteggio pari o superiore a 13 sulla scala Montgomery-Åsberg Depression Rating Scale (MADRS). (6) I ricercatori hanno evidenziato alcune differenze interessanti, nel gruppo trattato con probiotici:
- una lieve riduzione del livello di linfociti, unico marcatore infiammatorio a mostrare una variazione rilevante, e
- un miglioramento nel dominio neurovegetativo (ad esempio sonno e appetito), indicativo di un cambiamento clinicamente significativo (MCID), seppur minimo.
I probiotici, pur non risultando sufficienti come monoterapia per la riduzione dei sintomi depressivi, si sono rivelati promettenti come supporto integrativo ad altri trattamenti farmacologici o psicologici. È importante sottolineare che lo studio è stato condotto in una popolazione clinica ambulatoriale con depressione (prevenzione terziaria), contesto diverso rispetto ad altre ricerche svolte su soggetti sani o con depressione in comorbilità (prevenzione primaria e secondaria).
Né la dieta né i livelli di attività fisica hanno influenzato in modo significativo l’efficacia dell’intervento probiotico, che si è comunque dimostrato sicuro e ben tollerato alla dose utilizzata (3 × 10⁹ unità formanti colonie, CFU). Questo dosaggio risulta appropriato per interventi simili, pur lasciando spazio a potenziali ottimizzazioni basate su caratteristiche individuali — genetiche, sintomatologiche o metaboliche — come la selezione di specifici ceppi, loro combinazioni o una diversa durata del trattamento. Inoltre, la presenza di anomalie metaboliche più marcate (ad esempio sovrappeso o steatosi epatica) potrebbe attenuare i benefici psicometrici, forse a causa di una disbiosi sottostante che i probiotici mirano proprio a correggere.
Conclusioni provvisorie
Lo studio PRO-DEMET ha portato risultati innovativi sull’utilizzo dei probiotici in pazienti con sintomi depressivi. Le formulazioni di probiotici possono essere utilizzate come trattamento complementare efficace per i disturbi depressivi. La comorbilità con altri fattori come l’obesità o la steatosi epatica può influenzare l’efficacia dei trattamenti con probiotici per la depressione, l’ansia e lo stress. Tuttavia, sono essenziali ulteriori ricerche sui dettagli di tali interventi, anche tenendo conto di ulteriori studi su altri tipi di soggetti (es. sani con sintomi depressivi).
I primi risultati, seppure limitati, offrono opportunità interessanti per indirizzare la ricerca nello sviluppo di formulazioni precise di microrganismi probiotici in grado di migliorare lo stato di salute mentale. Un numero di partecipanti più elevato, e una maggiore considerazione di elementi di disturbo (es. percentuale di grasso corporeo, marker più accurati dello stato di infiammazione), devono essere inclusi in studi futuri.
Gli ostacoli forniti dalla Commissione europea non sono sicuramente utili ai consumatori, che vedono ristrette le possibilità di scegliere alimenti sicuri in grado di esercitare un effetto positivo sul microbiota intestinale e, di riflesso, sull’intero stato di salute, tra cui quello mentale.
Probiotici e salute, l’ostacolo europeo
La Commissione europea – con una decisione priva di valore legale, che confligge con le interpretazioni offerte da diversi Stati membri (es. Italia, Spagna) – ha associato il termine ‘probiotico‘ a una indicazione sulla salute, il cui utilizzo è vincolato a un’apposita autorizzazione preventiva ai sensi del Nutrition and Health Claims Regulation (EC) No 1924/06, NHCR. Tale decisione, come già approfondito su Food Times (Dongo, 2025):
- esprime un errore tecnico, poiché motivata con richiamo alla definizione di probiotico fornita da FAO (Food and Agriculture Organization) e WHO (World Health Organization) che riferisce la parola ‘health’ all’organismo ospite e non all’individuo (7);
- costringe gli operatori del settore ad affrontare enormi oneri per eseguire analisi sproporzionate (test in doppio cieco contro placebo su individui sani), ovvero rinunciare a informare i consumatori circa l’effettiva natura delle sostanze (probiotici), la quale invece trova esatta definizione e criteri di prova nel documento congiunto di FAO e WHO;
- penalizza gravemente gli investimenti nella ricerca e sviluppo in un settore che ha già mostrato un grande potenziale nel migliorare la salute delle persone, favorendo l’equilibrio (eubiosi) del microbiota intestinale;
- limita ingiustamente i diritti dei consumatori a identificare i prodotti che effettivamente contengono ingredienti probiotici, pregiudicando le loro possibilità di eseguire scelte informate di acquisto.
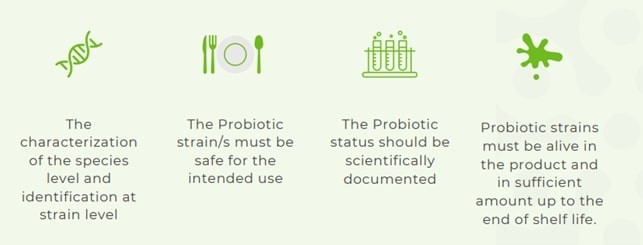
Fig. 2 – Requisiti suggeriti da IPA Europe per l’utilizzo del termine ‘probiotico’ (fonte: IPA Europe, 2025) (8)
International Probiotics Organisation (IPA) Europe ha a sua volta pubblicato un manifesto ove si sottolinea come il termine ‘probiotico’ è comunemente associato a una categoria di ingredienti alimentari che contengono microrganismi (in genere, batteri lattici e/o lieviti) vivi e vitali. Le sostanze che rispondono ai criteri internazionali stabiliti per definire i ‘probiotici‘ devono perciò poter venire denominate in quanto tali, per consentirne l’identificazione, senza che ciò comporti alcun suggerimento di benefici per la salute.
Dario Dongo e Andrea Adelmo Della Penna
Note
(1) Gawlik-Kotelnicka O. et al. (2021) The Influence of Probiotic Supplementation on Depressive Symptoms, Inflammation, and Oxidative Stress Parameters and Fecal Microbiota in Patients with Depression Depending on Metabolic Syndrome Comorbidity—PRO-DEMET Randomized Study Protocol. Journal of Clinical Medicine 10-1342, https://doi.org/10.3390/jcm10071342
(2) Gawlik-Kotelnicka O. et al. (2023) PRO-DEMET Randomized Controlled Trial on Probiotics in Depression—Pilot Study Results. Nutrients 15-1400, https://doi.org/10.3390/nu15061400
(3) Gawlik-Kotelnicka O. et al. (2024) Metabolic Status Influences Probiotic Efficacy for Depression—PRO-DEMET Randomized Clinical Trial Results. Nutrients 16-1389, https://doi.org/10.3390/nu16091389
(4) National Library of Medicine (U.S.). (2021, February 19). The influence of probiotic supplementation on depressive symptoms, inflammation, oxidative stress parameters and fecal microbiota in patients with depression depending on metabolic syndrome comorbidity. ClinicalTrials.gov. Identifier NCT04756544. https://clinicaltrials.gov/ct2/show/NCT04756544
(5) Si illustrano gli acronimi utilizzati nell’immagine: BMI – body mass index; BP – blood pressure; CBC – complete blood count; CRP – C-reactive protein; DASS – Depression, Anxiety, Stress Scale; fGlc – fasting glucose; HDL-c – high-density protein cholesterol; MADRS – Montgomery-Åsberg Depression Rating Scale; SCFAs – short-chain fatty acids; SQ – study questionnaire; TG – triglycerides; WC – waist circumference; WHOQOL-BREF – The World Health Organization quality of life-BREF
(6) Il MADRS è un questionario diagnostico utilizzato dai professionisti della salute mentale per misurare la gravità degli episodi depressivi in soggetti con disturbi dell’umore
(7) FAO/WHO. (2001). Health and nutritional properties of probiotics in food including powder milk with live lactic acid bacteria. Food and Agriculture Organization of the United Nations and World Health Organization Expert Consultation Report. http://www.fao.org/3/a-a0512e.pdf
(8) International Probiotics Association (IPA) Europe (2025). A holistic approach to probiotics in the EU for informed consumers and a sustainable food industry. https://tinyurl.com/4wzvsw8k
Bibliografia aggiuntiva
- Cerdó, T., García-Santos, J. A., Bermúdez, M. G., & Campoy, C. (2019). The role of probiotics and prebiotics in the prevention and treatment of obesity. Nutrients, 11(3), 635. https://doi.org/10.3390/nu11030635
- Dinan, T. G., & Cryan, J. F. (2017). The microbiome-gut-brain axis in health and disease. Gastroenterology Clinics of North America, 46(1), 77-89. https://doi.org/10.1016/j.gtc.2016.09.007
- Hill, C., Guarner, F., Reid, G., Gibson, G. R., Merenstein, D. J., Pot, B., Morelli, L., Canani, R. B., Flint, H. J., Salminen, S., Calder, P. C., & Sanders, M. E. (2014). Expert consensus document: The International Scientific Association for Probiotics and Prebiotics consensus statement on the scope and appropriate use of the term probiotic. Nature Reviews Gastroenterology & Hepatology, 11(8), 506-514. https://doi.org/10.1038/nrgastro.2014.66
- Ng, Q. X., Peters, C., Ho, C. Y. X., Lim, D. Y., & Yeo, W. S. (2018). A meta-analysis of the use of probiotics to alleviate depressive symptoms. Journal of Affective Disorders, 228, 13-19. https://doi.org/10.1016/j.jad.2017.11.063
- O’Mahony, S. M., Clarke, G., Borre, Y. E., Dinan, T. G., & Cryan, J. F. (2015). Serotonin, tryptophan metabolism and the brain-gut-microbiome axis. Behavioural Brain Research, 277, 32-48. https://doi.org/10.1016/j.bbr.2014.07.027
- Sarkar, A., Lehto, S. M., Harty, S., Dinan, T. G., Cryan, J. F., & Burnet, P. W. (2016). Psychobiotics and the manipulation of bacteria-gut-brain signals. Trends in Neurosciences, 39(11), 763-781. https://doi.org/10.1016/j.tins.2016.09.002
- Wallace, C. J. K., & Milev, R. (2017). The effects of probiotics on depressive symptoms in humans: A systematic review. Annals of General Psychiatry, 16, 14. https://doi.org/10.1186/s12991-017-0138-2